viernes, 30 de agosto de 2019
semana #26
REACCIONES ORGÁNICAS
Las reacciones orgánicas son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas. En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.
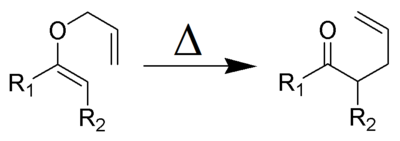
Ruptura de enlaces:
Las reacciones suponen que se lleve a cabo una ruptura de alguno de los enlaces que intervienen en las moléculas de las sustancias que reaccionan y la reordenación de los electrones de valencia para formar nuevos enlaces en los productos que da la reacción. Dichas rupturas, por lo general, pueden ocurrir en dos formas: ruptura hemolítica, y ruptura heterolítica.
Ruptura homolítica: Tiene lugar cuando un enlace de tipo covalente A:B se ve roto de manera que cada uno de los átomos se queda con un electrón del par del enlace. De esta manera, se consiguen dos radicales libres.
Dichas especies son neutras eléctricamente hablando, poseen un electrón que se encuentra desapareado, son bastante reactivas y cuentan con una vida media bastante corta.
La ruptura del enlace A:B tiene lugar así:
AB → A: + B∙
Ejemplo:
Este tipo de ruptura suele darse en compuestos que cuentan con una baja o incluso nula, polaridad y necesitan un suministro de energía que corresponda con la disociación del enlace.
Por esto, para poder iniciar la reacción a través de radicales libres se necesita un alto aporte a nivel energético. Dicha aportación puede llevarse a cabo a través de una vía térmica o también siguiendo un suministro de radiaciones. Estas reacciones generalmente tienen lugar en fase o estado gaseoso, o encontrándose en disolución con disolventes que sean no polares.
Ruptura heterolítica:
Se realiza cuando el enlace covalente A:B se rompe de maera que uno de los dos átomos que forma en enlace se quede con el par de electrones de este. De esta manera se consiguen dos iones, uno será positivo y el otro negativo.
La ruptura del enlace A:B se sucede así :
A:B → A+ + :B-
Cuando un carbono consigue conservar los dos electrones, el ion resultante recibe el nombre de carbanión R-, y en cambio, cuando los pierde se le denomina carbocatión R+. Es más frecuente la formación de un carbocatión que de un carboanión.
La ruptura heterolítica en un enlace covalente tiende a producirse en moléculas con una gran polaridad. Esta ruptura tiene lugar en condiciones más suaves que la ruptura homolítica, y por lo general, se da en presencia de disolventes polares que consiguen estabilizar a los iones.
Ya sean los radicales libres formados a partir de la ruptura homolítica como los iones que se dan en la ruptura heterolítica, reciben ambos el nombre de intermedios de reacción, e intervienen de manera general en los mecanismos de las reacciones de tipo orgánicas a modo de reactivos intermedios.
Clases de reactivos:
Es normal en las reacciones de la química orgánica llamar sustrato y reactivo a las distintas sustancias que participan en las reacciones. La molécula que reacciona, generalmente es la mayor, y se llama sustrato. Esta será atacada por otra molécula, por lo general más pequeña, llamada reactivo, que dará lugar a la reacción química al interaccionar con el sustrato. Dicho reactivo, puede ser de distintas naturalezas, inorgánico, radical libre, electrófilo o nucleófilo.
– Radicales libres
se producen en las reacciones homolíticas, son bastante reactivos e interaccionan con otros tipos de radicales o con moléculas de tipo neutro. Los radicales en química orgánica se llaman primarios, secundarios o terciarios, dependiendo de la naturaleza que tenga el carbono que cuente con el electrón no apareado. Los radicales terciarios son los que mas estabilidad poseen, y por lo tanto, son menos reactivos.
– Reactivos electrófilos:
Son reactivos con alguno de sus átomos de poca densidad electrónica, por lo cual suelen actuar sobre los átomos del sustrato que tienen carga negativa, o una alta densidad de carga. Los reactivos electrófilos siempre son cationes u otras moléculas que tienen algún orbital atómico sin ocupar, como por ejemplo H+, BF3, SO3, etc.
– Reactivos nucleófilos: Son reactivos que tienen algunos de sus átomos con una alta densidad de carga, por lo que suelen actuar en los átomos del sustrato que tenga carga positiva o un déficit de carga. Por lo general son aniones o neutros con electrones libres, por lo tanto, ceden electrones. Es el caso del H-, OH-, CN-, etc.
Principales tipos de reacciones orgánicas:
Si tenemos en cuenta la relación que existe entre el sustrato y los productos de la reacción, podemos distinguir diferentes tipos de reacciones orgánicas. Destacamos las reacciones de sustitución, de adición, de eliminación, de condensación, así como las reacciones de polarización.
–Reacciones de sustitución
Son reacciones donde un átomo o varios átomos de un reactivo se meten en la cadena de carbonos que forma al sustrato, consiguiendo cambiar alguno de los átomos que se encuentran unidos al carbono.
R-X (sustrato) + Y ( reactivo) → R-Y + X
Según el tipo de ruptura que se cree en los enlaces, la sustitución podrá ser homolítica o heterolítica. La más frecuente es la sustitución heterolítica, la cual además puede ser nucleófila o electrófila (SN1, SN2, E1, o E2).
Las reacciones orgánicas son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas. En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.

Ruptura de enlaces:
Las reacciones suponen que se lleve a cabo una ruptura de alguno de los enlaces que intervienen en las moléculas de las sustancias que reaccionan y la reordenación de los electrones de valencia para formar nuevos enlaces en los productos que da la reacción. Dichas rupturas, por lo general, pueden ocurrir en dos formas: ruptura hemolítica, y ruptura heterolítica.
Ruptura homolítica: Tiene lugar cuando un enlace de tipo covalente A:B se ve roto de manera que cada uno de los átomos se queda con un electrón del par del enlace. De esta manera, se consiguen dos radicales libres.
Dichas especies son neutras eléctricamente hablando, poseen un electrón que se encuentra desapareado, son bastante reactivas y cuentan con una vida media bastante corta.
La ruptura del enlace A:B tiene lugar así:
AB → A: + B∙
Ejemplo:
Este tipo de ruptura suele darse en compuestos que cuentan con una baja o incluso nula, polaridad y necesitan un suministro de energía que corresponda con la disociación del enlace.
Por esto, para poder iniciar la reacción a través de radicales libres se necesita un alto aporte a nivel energético. Dicha aportación puede llevarse a cabo a través de una vía térmica o también siguiendo un suministro de radiaciones. Estas reacciones generalmente tienen lugar en fase o estado gaseoso, o encontrándose en disolución con disolventes que sean no polares.
Ruptura heterolítica:
Se realiza cuando el enlace covalente A:B se rompe de maera que uno de los dos átomos que forma en enlace se quede con el par de electrones de este. De esta manera se consiguen dos iones, uno será positivo y el otro negativo.
La ruptura del enlace A:B se sucede así :
A:B → A+ + :B-
Cuando un carbono consigue conservar los dos electrones, el ion resultante recibe el nombre de carbanión R-, y en cambio, cuando los pierde se le denomina carbocatión R+. Es más frecuente la formación de un carbocatión que de un carboanión.
La ruptura heterolítica en un enlace covalente tiende a producirse en moléculas con una gran polaridad. Esta ruptura tiene lugar en condiciones más suaves que la ruptura homolítica, y por lo general, se da en presencia de disolventes polares que consiguen estabilizar a los iones.
Ya sean los radicales libres formados a partir de la ruptura homolítica como los iones que se dan en la ruptura heterolítica, reciben ambos el nombre de intermedios de reacción, e intervienen de manera general en los mecanismos de las reacciones de tipo orgánicas a modo de reactivos intermedios.
Clases de reactivos:
Es normal en las reacciones de la química orgánica llamar sustrato y reactivo a las distintas sustancias que participan en las reacciones. La molécula que reacciona, generalmente es la mayor, y se llama sustrato. Esta será atacada por otra molécula, por lo general más pequeña, llamada reactivo, que dará lugar a la reacción química al interaccionar con el sustrato. Dicho reactivo, puede ser de distintas naturalezas, inorgánico, radical libre, electrófilo o nucleófilo.
– Radicales libres
se producen en las reacciones homolíticas, son bastante reactivos e interaccionan con otros tipos de radicales o con moléculas de tipo neutro. Los radicales en química orgánica se llaman primarios, secundarios o terciarios, dependiendo de la naturaleza que tenga el carbono que cuente con el electrón no apareado. Los radicales terciarios son los que mas estabilidad poseen, y por lo tanto, son menos reactivos.
– Reactivos electrófilos:
Son reactivos con alguno de sus átomos de poca densidad electrónica, por lo cual suelen actuar sobre los átomos del sustrato que tienen carga negativa, o una alta densidad de carga. Los reactivos electrófilos siempre son cationes u otras moléculas que tienen algún orbital atómico sin ocupar, como por ejemplo H+, BF3, SO3, etc.
– Reactivos nucleófilos: Son reactivos que tienen algunos de sus átomos con una alta densidad de carga, por lo que suelen actuar en los átomos del sustrato que tenga carga positiva o un déficit de carga. Por lo general son aniones o neutros con electrones libres, por lo tanto, ceden electrones. Es el caso del H-, OH-, CN-, etc.
Principales tipos de reacciones orgánicas:
Si tenemos en cuenta la relación que existe entre el sustrato y los productos de la reacción, podemos distinguir diferentes tipos de reacciones orgánicas. Destacamos las reacciones de sustitución, de adición, de eliminación, de condensación, así como las reacciones de polarización.
–Reacciones de sustitución
Son reacciones donde un átomo o varios átomos de un reactivo se meten en la cadena de carbonos que forma al sustrato, consiguiendo cambiar alguno de los átomos que se encuentran unidos al carbono.
R-X (sustrato) + Y ( reactivo) → R-Y + X
Según el tipo de ruptura que se cree en los enlaces, la sustitución podrá ser homolítica o heterolítica. La más frecuente es la sustitución heterolítica, la cual además puede ser nucleófila o electrófila (SN1, SN2, E1, o E2).
semana #25
ISOMERIA CONFORMACIONAL
La libre rotación en torno a un enlace simple da lugar a que las moléculas puedan adoptar un número infinito de distribuciones espaciales interconvertibles recíprocamente sin ruptura de enlaces, debido a que entre los carbonos, se encuentra un enlace sencillo o sigma (σ). Estas disposiciones espaciales reciben el nombre genérico de conformaciones, y las distintas conformaciones reciben el nombre de confórmeros.
Alternada: Es la más estable (menor energía) pues sus átomos están los más separados posible y por tanto la interacción es mínima.
Eclipsada: Es la menos estable (mayor energía).
Sesgada o desviada: Se llaman así a las infinitas conformaciones que existen entre la alternada y la eclipsada. Su energía es mayor que la alternada y menor que la eclipsada.
La rotación del enlace carbono-carbono en el etano da lugar a dos conformaciones límite:
-La conformaciones alternada (con los hidrógenos alternados)
- La conformación eclipsada (con los hidrógenos enfrentados)
- El paso de la conformación alternada a la eclipsada o viceversa se realiza por giro de 60º. Obsérvese que en un giro de 360º existen infinitas conformaciones posibles.




La libre rotación en torno a un enlace simple da lugar a que las moléculas puedan adoptar un número infinito de distribuciones espaciales interconvertibles recíprocamente sin ruptura de enlaces, debido a que entre los carbonos, se encuentra un enlace sencillo o sigma (σ). Estas disposiciones espaciales reciben el nombre genérico de conformaciones, y las distintas conformaciones reciben el nombre de confórmeros.
Alternada: Es la más estable (menor energía) pues sus átomos están los más separados posible y por tanto la interacción es mínima.
Eclipsada: Es la menos estable (mayor energía).
Sesgada o desviada: Se llaman así a las infinitas conformaciones que existen entre la alternada y la eclipsada. Su energía es mayor que la alternada y menor que la eclipsada.
La rotación del enlace carbono-carbono en el etano da lugar a dos conformaciones límite:
-La conformaciones alternada (con los hidrógenos alternados)
- La conformación eclipsada (con los hidrógenos enfrentados)
- El paso de la conformación alternada a la eclipsada o viceversa se realiza por giro de 60º. Obsérvese que en un giro de 360º existen infinitas conformaciones posibles.
Para el análisis de estas conformaciones, se utilizan las Proyecciones de Newman, que se representan de la siguiente manera:
En estas proyecciones, el grupo más cercano al observador se representa como:

El grupo más lejano al observador se representa como:

Entonces

En el Etano, que es uno de los casos más sencillos de considerar, las conformaciones más notables son la alternada y la eclipsada. La más estable, siempre será la que tenga menor energía, que en este caso es la Alternada como se muestra a continuación:
semana #24
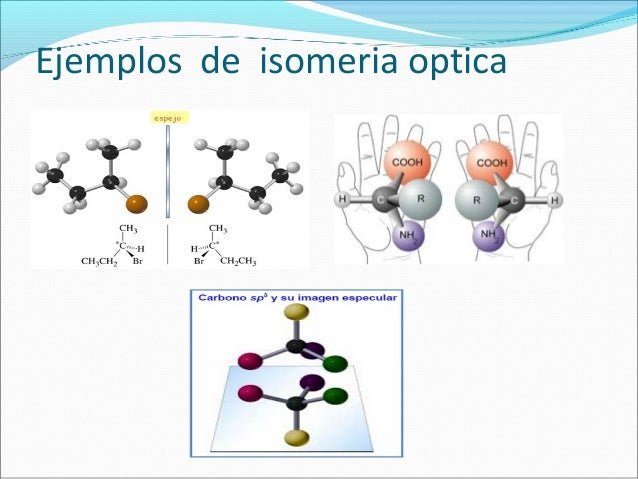
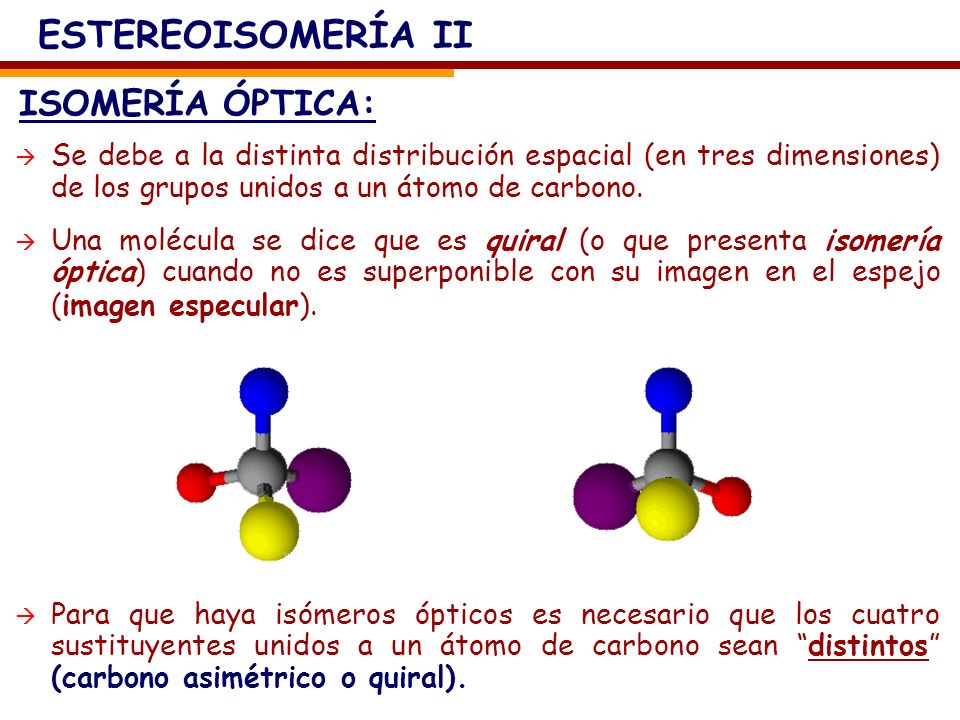
Isomeria Óptica
Existen moléculas que coinciden en todas sus propiedades excepto en su capacidad de desviar el plano de luz polarizada. Son los llamados isómeros ópticos.
semana #23
Isomeria cis-trans
La isomería cis-trans o geométrica es debida a la rotación restringida entorno a un enlace carbono-carbono. Esta restricción puede ser debida a la presencia de dobles enlaces o ciclos. Así, el 2-buteno puede existir en forma de dos isómeros, llamados cis y trans. El isómero que tiene los hidrógenos al mismo lado se llama cis, y el que los tiene a lados opuestos trans.
Isómeros geométricos o cis - trans

Los compuestos cíclicos, debido a su rigidez, también presentan isomería geométrica. Así, el 1,2-dimetilciclohexano puede existir en forma de dos isómeros. Se llama isómero cis el que tiene los hidrógenos al mismo lado y trans el que los tiene a lados opuestos.

semana #22
Definición de isómeros
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.

Isómeros de posición
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.

Isómeros de función
El grupo funcional es diferente. El 2-butanol y el dietil éter presentan la misma fórmula molecular, pero pertenecen a familias diferentes -alcohol y éter- por ello se clasifican como isómeros de función.

Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.

Isómeros de posición
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.

Isómeros de función
El grupo funcional es diferente. El 2-butanol y el dietil éter presentan la misma fórmula molecular, pero pertenecen a familias diferentes -alcohol y éter- por ello se clasifican como isómeros de función.

semana #21
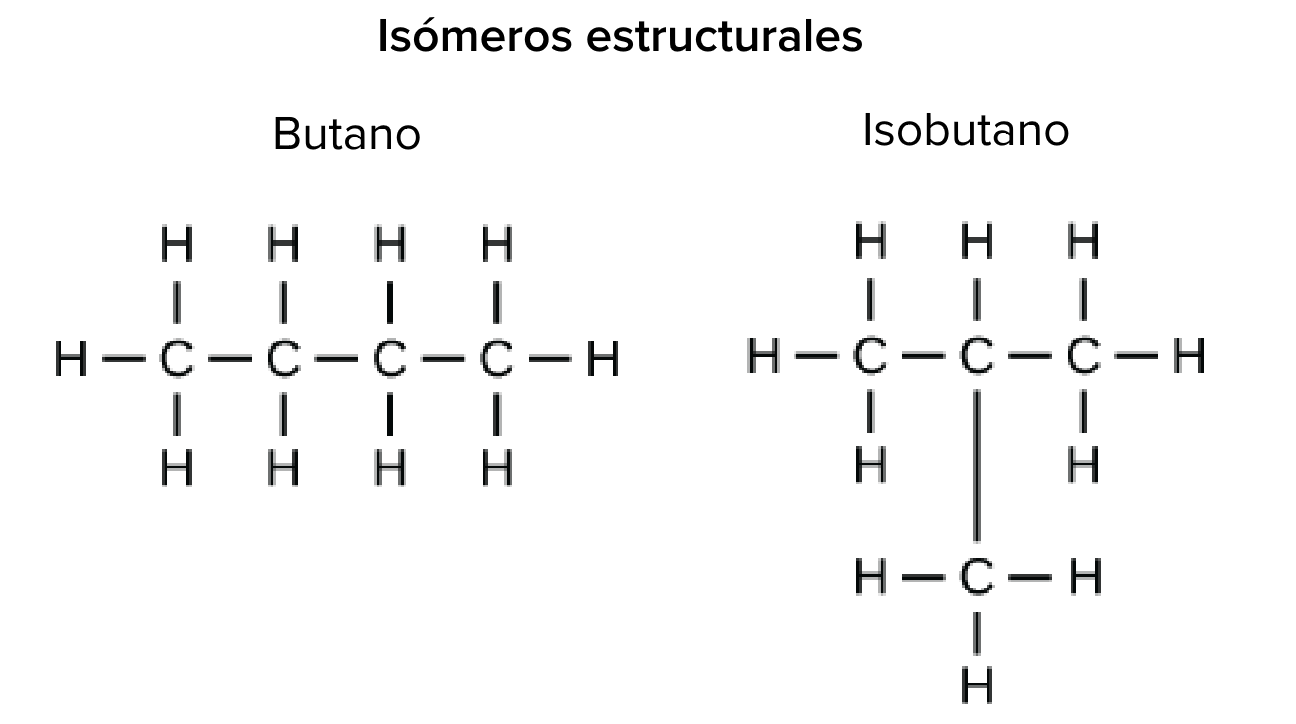
Isomeros Estructurales
La isomería es usada para denominar a aquellos compuestos que aun teniendo el mismo número y clase de átomos(fórmula molecular), muestran una distinta ordenación de los átomos en la molécula. Imaginen que su querida progenitora (aka madre) les compra el mismo tipo y cantidad de frutas para que ambos puedan disfrutarlas en el carro, al momento de acomodarlas ya sea en cualquier espacio adecuado en el coche; es muy probable que ella las acomode en un orden distinto, incluso en un lugar distinto al suyo. Por lo que ambos tienen lo mismo pero en un orden diferente. Pues así mismo ocurre con los átomos de estos compuestos, tienen una composición idéntica más su orden varía.
semana #18
Primera clase : se hace repaso y luego se realiza quiz ( a partir del nombre hacer la estructura).
Segunda clase: Se hace repaso y luego se realiza quiz( a partir de la estructura hacer el nombre )
Segunda clase: Se hace repaso y luego se realiza quiz( a partir de la estructura hacer el nombre )
semana # 16
DADA LA ESTRUCTURA ENCONTRAR CADA UNA DE LAS PARTES DEL NOMBRE, JUNTARLAS Y NOMBRARLAS.
° 4-etiliden-6-vinilnona-2,7-dieno

° 4-etiliden-6-vinilnona-2,7-dieno

semana #15
se continúan los ejemplos del documento :
°ciclo hexil ciclo hexano
CH₂ - CH₂
/ \
CH₂ CH₂ ------> Ciclohexil
\ /
CH - CH₂
|
CH - CH₂
/ \
CH₂ CH₂ --------> Ciclohexano
\ /
CH₂ - CH₂
°5-etil-4,6dimetil/oct/a-4-en-2,7-diino-1,6-ditiol
H CH3
| |
HS - C - C - C -C - C- C-C-C-H
| | |
CH3 CH2 SH
|
CH3
raiz: oct
prefijo 1:lineal
prefijo 2: 5 etil-4,6-dimetil
sufijo 1:4-en-2,7-diino
sufijo 2: 1,6 -ditiol
semana #14
ejercicios del documento:
A partir del nombre hacer la estructura:
° 4- met/oxi/ciclo/hex/an/carboxaldehido
raiz: hex
prefijo:1 ciclo
sufijo: etanal
° Acido- 4- metil-2-ceto-3,3 di ( 1-metil/etenil)-4-pentenoico
C--CH2
|
C -- C - C - C - C // O
| | || |
CH3 C O OH
| - CH2
CH3
raiz:pent
sufijo:en
° ( N-2,4 -dinitro fenil ) 3,4 -dimeti-1-ciclopent/eno/carboxiamida
° 3,7- dietril-4,8-dimetil-5-(1,1,2 -trimetril/prop/il)- 2,5- non/adieno
H H H H H
| | | | |
H3C - CH2 - C - C -C - C - C - C - CH3
| | | | | |
CH2 CH3 C H CH2 CH3
CH3 H
| |
C- C- CH3
| |
CH3 CH3
° 2,3,4-trimetilpentano

A partir del nombre hacer la estructura:
° 4- met/oxi/ciclo/hex/an/carboxaldehido
raiz: hex
prefijo:1 ciclo
sufijo: etanal
° Acido- 4- metil-2-ceto-3,3 di ( 1-metil/etenil)-4-pentenoico
C--CH2
|
C -- C - C - C - C // O
| | || |
CH3 C O OH
| - CH2
CH3
raiz:pent
sufijo:en
° ( N-2,4 -dinitro fenil ) 3,4 -dimeti-1-ciclopent/eno/carboxiamida
° 3,7- dietril-4,8-dimetil-5-(1,1,2 -trimetril/prop/il)- 2,5- non/adieno
H H H H H
| | | | |
H3C - CH2 - C - C -C - C - C - C - CH3
| | | | | |
CH2 CH3 C H CH2 CH3
CH3 H
| |
C- C- CH3
| |
CH3 CH3
° 2,3,4-trimetilpentano

semana #13
LA MOTIVACIÓN:
La motivación es muy importante,porque nos lleva a buscar activamente los recursos para garantizar nuestra subsistencia.
Nos lleva a cumplir nuestros sueños y metas.
SE CONTINÚAN HACIENDO EJEMPLOS

a.
OH = función principal
|
CH3-CH--CH-CH2-CH-CH3
raiz: Hex
suf. 1°: 4 - en 4-hexen-2-ol
fuf. 2°: ol
b.
1 2 3 4 5 6 7
CH3 - C - CH2- CH- C- CH2- CH3
|| | ||
O OH O
2,5-diona
4-hidroxi 4-hidroxi-2,5- heptanodiona
raiz:hept
suf. 1° : an - sencillo
suf.2° : 2,5 - diona
prefijo 1 ° : lineal
prefijo 2° : 4- hidroxi
c. O O
|| ||
C - CH2 - CH - CH2 - CH2 - C - OH
|
OH
raiz: hex
sufijo 1 : an
sufijo 2 : 1,6 - dioico
prefijo 2: hidroxi
Segunda clase:
Compuestos aromáticos:
Son aquellos que presentan aromas algunas veces son agradables y otras veces desagradables.
ejemplo: la escencias de vainilla,canela y olores desagradables
¿que es aromaticidad?
la aromaticidad se presenta cuando existe enlaces dobles conjugados que permiten la deslocalización electrónica.
ciclo parafenol:

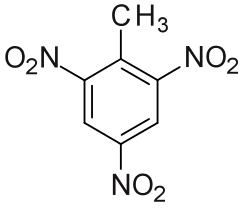
trinitrotolueno:
La motivación es muy importante,porque nos lleva a buscar activamente los recursos para garantizar nuestra subsistencia.
Nos lleva a cumplir nuestros sueños y metas.
SE CONTINÚAN HACIENDO EJEMPLOS

a.
OH = función principal
|
CH3-CH--CH-CH2-CH-CH3
raiz: Hex
suf. 1°: 4 - en 4-hexen-2-ol
fuf. 2°: ol
b.
1 2 3 4 5 6 7
CH3 - C - CH2- CH- C- CH2- CH3
|| | ||
O OH O
2,5-diona
4-hidroxi 4-hidroxi-2,5- heptanodiona
raiz:hept
suf. 1° : an - sencillo
suf.2° : 2,5 - diona
prefijo 1 ° : lineal
prefijo 2° : 4- hidroxi
c. O O
|| ||
C - CH2 - CH - CH2 - CH2 - C - OH
|
OH
raiz: hex
sufijo 1 : an
sufijo 2 : 1,6 - dioico
prefijo 2: hidroxi
Segunda clase:
Compuestos aromáticos:
Son aquellos que presentan aromas algunas veces son agradables y otras veces desagradables.
ejemplo: la escencias de vainilla,canela y olores desagradables
¿que es aromaticidad?
la aromaticidad se presenta cuando existe enlaces dobles conjugados que permiten la deslocalización electrónica.
ciclo parafenol:

trinitrotolueno:

semana #12
Sufijo secundario : Están ordenados,según lo establecido convencionalmente por la I.U.P.A.C , en orden decreciente de importancia .
Cadena principal o raíz : Es a secuencia carbonada progenitora del compuesto particular y equivale al hidrocarburo no ramificado del mismo numero de atomos de carbono.
Si poseen un radical se toma el nombre del ciclo como la cadena principal:
Etilciclopentano Metilciclobutano Propilciclohexeno
Selección : La secuencia principal debe ser la cadena continua mas extensa de átomos de carbono que cumple el siguiente orden de prioridades , incluyendo :
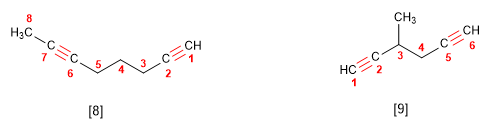
a. el mayor numero de veces la función principal
Resultado de imagen para funciones principales quimica
tabla15
b. el mayor numero de instauraciones con predominio del enlace doble sobre el triple.
Resultado de imagen para predominio del enlace doble sobre el triple
c. el mayor numero de otros grupos funcionales y sustituyentes en general .
Resultado de imagen para el mayor numero de otros grupos funcionales y sustituyentes en general
se realizaron ejemplos de algunos hidrocarburos :
Org_1_1

Numeración de la secuencia principal:

semana #11
NOMENCLATURA DE H.C RAMIFICADOS Y ESTRUCTURAS COMPLEJAS :
normas: I.U.P.A.C : unión internacional de la química pura y aplicada .
nomenclatura :lenguaje de la química - nombres de los compuestos (sistemático)
Nombres comunes :
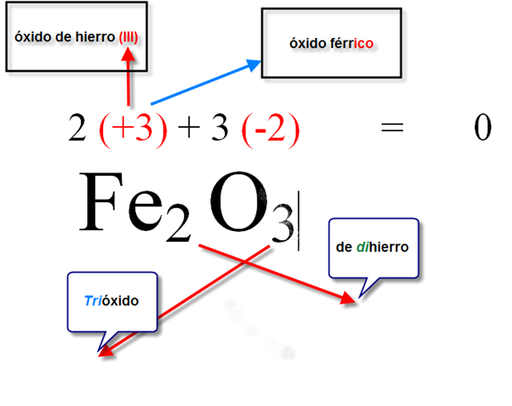
PREFIJOS - RAÍZ-SUFIJOS :
raíz: Numero de carbonos de la cadena principal .
MET/AN/O
raíz :met
an: sufijo
o: sufijo 2

normas: I.U.P.A.C : unión internacional de la química pura y aplicada .
nomenclatura :lenguaje de la química - nombres de los compuestos (sistemático)
Nombres comunes :

PREFIJOS - RAÍZ-SUFIJOS :
raíz: Numero de carbonos de la cadena principal .
MET/AN/O
raíz :met
an: sufijo
o: sufijo 2

semana #6
Quiz de las leyes de los gases
Hibridación del Carbono

Hibridación del Carbono
La hibridación del carbono implica la combinación de dos orbitales atómicos puros para formar un nuevo orbital molecular “híbrido” con características propias. La noción de orbital atómico da una mejor explicación que el concepto anterior de órbita, para establecer una aproximación de dónde hay mayor probabilidad de hallar un electrón dentro de un átomo.
Estos parámetros son únicos para cada electrón en un orbital, por lo que dos electrones no pueden tener exactamente los mismos valores de los cuatro números cuánticos y cada orbital puede ser ocupado por dos electrones como máximo.
Dicho de otra forma, un orbital atómico es la representación de la mecánica cuántica para dar una idea de la posición de un electrón o par de electrones en una zona determinada dentro del átomo, donde cada orbital se define de acuerdo con los valores de sus números cuánticos.

Los números cuánticos describen el estado de un sistema (como el del electrón dentro del átomo) en determinado momento, por medio de la energía perteneciente al electrón (n), el momento angular que describe en su movimiento (l), el momento magnético relacionado (m) y el giro del electrón mientras se desplaza dentro del átomo (s).
Tipos principales:
Sp3
(Cuatro regiones de densidad electrónica alrededor del C)
 Un carbono unido a cuatro átomos siempre tendrá hibridación sp3 y una estructura tetraédrica. Así son los alcanos, haluros de alquilo, alcoholes, éteres y aminas, entre otros. Todos estos compuestos tienen estabilidad suficiente como para poder ser almacenados sin problemas especiales. Un carbono unido a menos de cuatro átomos también puede tener hibridación sp3 pero la estructura variará dependiendo del número de sustituyentes:
Los carbaniones y carbenos son especies altamente reactivas (intermedios de reacción) y en general tienen un tiempo de vida muy corto.
|
sp2
(Tres regiones de densidad electrónica alrededor del C) 
Un carbono unido a tres átomos, que mantiene un doble enlace con uno de ellos, siempre tendrá hibridación sp2 y una geometría trigonal plana. Así son compuestos estables tales como olefinas, hidrocarburos aromáticos, aldehídos, cetonas y ácidos carboxílcos y derivados, entre otros.
Existen otras situaciones donde un átomo de carbono unido a tres átomos también posee hibridación sp2:
Carbocationes y radicales son especies altamente reactivas (intermedios de reacción) y en general tienen un tiempo de vida muy corto.
|
sp
(Dos regiones de densidad electrónica alrededor del C)  
Un carbono unido a dos átomos, que mantiene un triple enlace con uno de ellos, siempre tendrá una hibridación sp y una estructura lineal.
Existen otras posibilidades:
¿Qué son los Alcanos?
Los Alcanos (también llamados Parafinas o Hidrocarburos Saturados) son compuestos orgánicos del grupo de los Hidrocarburos, es decir, que están formados únicamente por átomos de carbono e hidrógeno. Lo que diferencia a los Alcanos del resto de Hidrocarburos es que sus átomos de carbono están unidos por enlaces sencillos.
CnH2n+2
Ejemplos
1. PENTANO (C5H12)
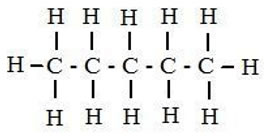 2.ISOPENTANO O 2-METILBUTANO (C5H12) 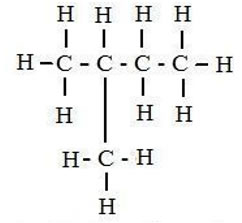 3. 2,2 DIMETILPROPANO (C5H12) 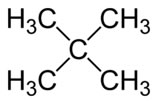 4. 3-metilpentano (C6H14) 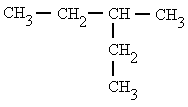
5. 4-etil-2,4-dimetilhexano (C12H26)
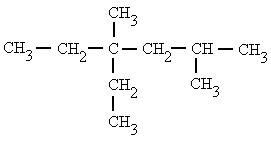
6.3-isopropil-2,5-dimetilheptano
|
Suscribirse a:
Comentarios (Atom)






