Hibridación del Carbono
La hibridación del carbono implica la combinación de dos orbitales atómicos puros para formar un nuevo orbital molecular “híbrido” con características propias. La noción de orbital atómico da una mejor explicación que el concepto anterior de órbita, para establecer una aproximación de dónde hay mayor probabilidad de hallar un electrón dentro de un átomo.
Estos parámetros son únicos para cada electrón en un orbital, por lo que dos electrones no pueden tener exactamente los mismos valores de los cuatro números cuánticos y cada orbital puede ser ocupado por dos electrones como máximo.
Dicho de otra forma, un orbital atómico es la representación de la mecánica cuántica para dar una idea de la posición de un electrón o par de electrones en una zona determinada dentro del átomo, donde cada orbital se define de acuerdo con los valores de sus números cuánticos.

Los números cuánticos describen el estado de un sistema (como el del electrón dentro del átomo) en determinado momento, por medio de la energía perteneciente al electrón (n), el momento angular que describe en su movimiento (l), el momento magnético relacionado (m) y el giro del electrón mientras se desplaza dentro del átomo (s).
Tipos principales:
Sp3
(Cuatro regiones de densidad electrónica alrededor del C)
 Un carbono unido a cuatro átomos siempre tendrá hibridación sp3 y una estructura tetraédrica. Así son los alcanos, haluros de alquilo, alcoholes, éteres y aminas, entre otros. Todos estos compuestos tienen estabilidad suficiente como para poder ser almacenados sin problemas especiales. Un carbono unido a menos de cuatro átomos también puede tener hibridación sp3 pero la estructura variará dependiendo del número de sustituyentes:
Los carbaniones y carbenos son especies altamente reactivas (intermedios de reacción) y en general tienen un tiempo de vida muy corto.
|
sp2
(Tres regiones de densidad electrónica alrededor del C) 
Un carbono unido a tres átomos, que mantiene un doble enlace con uno de ellos, siempre tendrá hibridación sp2 y una geometría trigonal plana. Así son compuestos estables tales como olefinas, hidrocarburos aromáticos, aldehídos, cetonas y ácidos carboxílcos y derivados, entre otros.
Existen otras situaciones donde un átomo de carbono unido a tres átomos también posee hibridación sp2:
Carbocationes y radicales son especies altamente reactivas (intermedios de reacción) y en general tienen un tiempo de vida muy corto.
|
sp
(Dos regiones de densidad electrónica alrededor del C)  
Un carbono unido a dos átomos, que mantiene un triple enlace con uno de ellos, siempre tendrá una hibridación sp y una estructura lineal.
Existen otras posibilidades:
¿Qué son los Alcanos?
Los Alcanos (también llamados Parafinas o Hidrocarburos Saturados) son compuestos orgánicos del grupo de los Hidrocarburos, es decir, que están formados únicamente por átomos de carbono e hidrógeno. Lo que diferencia a los Alcanos del resto de Hidrocarburos es que sus átomos de carbono están unidos por enlaces sencillos.
CnH2n+2
Ejemplos
1. PENTANO (C5H12)
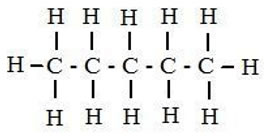 2.ISOPENTANO O 2-METILBUTANO (C5H12) 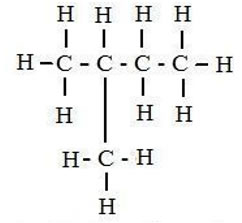 3. 2,2 DIMETILPROPANO (C5H12) 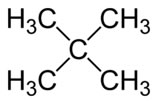 4. 3-metilpentano (C6H14) 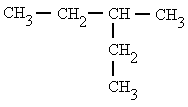
5. 4-etil-2,4-dimetilhexano (C12H26)
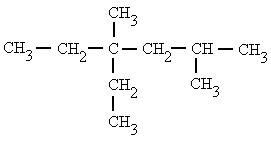
6.3-isopropil-2,5-dimetilheptano
|






No hay comentarios.:
Publicar un comentario